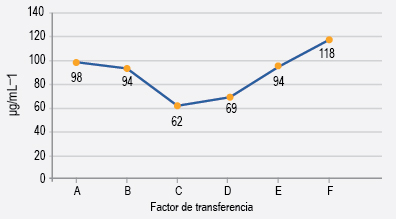
Figura 1. Análisis del contenido proteico de los FT estudiados, cuantificado por el método de Bradford. Los valores se obtuvieron a partir de una curva de referencia de un estándar de albúmina de concentración conocida.
ARTÍCULO ORIGINAL
Guillermo Arturo Guidos-Fogelbach,1 Jorge Antonio Paredes-Aguilar,1 Nayeli Montserrat Colín-Martínez,1 María Isabel Rojo-Gutiérrez,2 Marisol López-Hidalgo,1 César Augusto Sandino Reyes-López1
1Instituto Politécnico Nacional, Escuela Nacional de Medicina y Homeopatía, Laboratorio de Bioquímica Estructural. Ciudad de México, México
2Secretaría de Salud, Hospital Juárez de México, Servicio de Alergia e inmunología. Ciudad de México, México
Este artículo debe citarse como: Guidos-Fogelbach GA, Paredes-Aguilar JA, Colín-Martínez NM, Rojo-Gutiérrez MI, López-Hidalgo M, Reyes-López CAS. Determinación y análisis del perfil proteico de diferentes factores de transferencia. Rev Alerg Mex. 2016;63(4):365-372.
Introducción: El factor de transferencia (FT) es el extracto dializable de leucocitos con propiedades de transferencia de inmunidad celular. Su uso se ha extendido en el tratamiento de una amplia gama de padecimientos inmunológicos, infecciosos y como coadyuvante de padecimientos oncológicos. A pesar de ello, no se conocen completamente aspectos importantes de su perfil proteico, concentraciones de componentes y mecanismos de acción.
Objetivos: Analizar los perfiles proteicos de diferentes factores de transferencia comercializados en México.
Métodos: Se obtuvieron y analizaron 6 FT comercializados en México. Se realizó la cuantificación de proteínas por el método de Bradford, cromatografía líquida de alta resolución (HPLC) y electroforesis en geles de poliacrilamida (SDS-PAGE). Todas las muestras fueron analizadas por duplicado.
Resultados: Las concentraciones de proteínas totales de todos los FT analizados fueron menores de 0.2 mg/mL. Los perfiles cromatográficos mostraron diferencias en algunos FT. La concentración de proteínas resultó de 6 hasta casi mil veces más baja en comparación con lo informado por algunos fabricantes.
Conclusión: Casi la totalidad de los factores de transferencia comercializados en México carecen de un etiquetado y registro sanitario que cumpla con las normas oficiales vigentes.
Palabras clave: Factor de transferencia; Análisis proteico
How to cite this article: Guidos-Fogelbach GA, Paredes-Aguilar JA, Colín-Martínez NM, Rojo-Gutiérrez MI, López-Hidalgo M, Reyes-López CAS. [Determination and analysis of protein profile of different transfer factors]. Rev Alerg Mex. 2016;63 Oct-Dec(4):365-372.
Background: The transfer factor (TF) is the dialyzable extract of leukocytes with cellular immunity transfer properties. Its use has spread in the treatment of a wide range of immunologic, infectious, and even oncological diseases. However, important aspects in their protein profile, component concentrations, and a well-defined action mechanism are not completely unknown.
Objectives: To analyze the protein profiles of different transfer factors marketed in Mexico.
Methods: 6 TF marketed in Mexico were obtained and analyzed, quantifying protein with thaze Bradford method, by high-performance liquid chromatography (HPLC), and polyacrylamide gel electrophoresis (SDS-PAGE). All samples were analyzed in duplicate.
Results: The total protein concentrations of all TF analyzed are less than 0.2 mg/mL. The chromatographic profiles showed differences in some TF. The protein concentration was 6 to almost one thousand times lower compared to reports by some manufacturers.
Conclusion: Almost all transfer factors marketed in Mexico lack a labeling and health record that meets the official standards.
Keywords: Transfer factor; Protein analysis
Abreviaturas y siglas
AMPc, adenosin monofosfato cíclico
FT, factor de transferencia
FTE, factores de transferencia específicos
HPLC, cromatografía líquida de alta resolución
IL-2rα, receptor α para interleucina 2
IL-6, interleucina 6
IL-8, interleucina 8
INFγ: interferón γ
NF-κβ, factor nuclear κβ
SDS-PAGE, electroforesis en geles de poliacrilamida en condiciones desnaturalizantes
TFA, ácido trifluroacético
TLR 2, receptor tipo toll 2
TNFα, factor de necrosis tumoral α
TRL 4, receptor tipo toll 4
El factor de transferencia (FT), descrito por Henry S. Lawrence en 1949, es un conjunto de alrededor de 200 moléculas peptídicas con funciones moduladoras del sistema inmunológico con un peso molecular menor a 10 kDa, actúan sobre los canales de calcio como mensajeros que transmiten información inmunológica producida por los linfocitos T como parte de la inmunidad celular. En 1956, H. S. Lawrence y Pappenheimer describieron que el FT era capaz de transmitir memoria inmunitaria de forma independiente de la inmunidad humoral dada por los anticuerpos.1-4
Charles H. Kirkpatrick identificó la secuencia consenso de aminoácidos del FT y describió que era altamente conservada, independientemente de las fuentes y especies de obtención.5,6
En la actualidad, los FT se purifican, liofilizan y se encapsulan para su consumo. Los preparados de FT pueden incluir productos completos o parciales gracias a tecnologías de microfiltración.6 Los extractos de FT son complejos y contienen más de 200 moléculas con pesos moleculares de 1 a 20 kDa; algunas de estas son proteínas con pesos moleculares entre 3.5 y 5 kDa específicas de antígeno, que se denominan factores de transferencia específicos (FTE).
En la práctica clínica, el FT se emplea como un adyuvante inmunológico para el manejo de una amplia gama de enfermedades que van desde hipersensibilidades tipo 1, inmunodeficiencias primarias y secundarias, cáncer, procesos infecciosos, alteraciones cutáneas, entre otros, por lo que su uso y comercialización se ha masificado en México y en otros países.7-19
A pesar de esto, su mecanismo de acción no se encuentra totalmente esclarecido, pero se postula que está implicada la modificación de la señalización de la respuesta inmune innata (↑TLR 2, ↑TRL 4, ↑IL-2rα, NF-κβ), lo que origina la elevación de los niveles de TNFα, IL-6, IL-8, INFγ y AMPc,20-22 sin embargo, no se cuenta con una regulación de las fuentes de obtención, composición proteica y esquemas terapéuticos.22
Objetivos
Analizar los perfiles proteicos de los diferentes FT comercializados en México por los siguientes métodos: cuantitativo de Bradford, cromatografía líquida de alta resolución (HPLC) y electroforesis en geles de poliacrilamida en condiciones desnaturalizantes (SDS-PAGE).
La investigación se realizó en el Laboratorio de Bioquímica Estructural, Sección de Estudios de Postgrado e Investigación, Escuela Nacional de Medicina y Homeopatía, Instituto Politécnico Nacional, Ciudad de México. Se obtuvieron extractos comerciales de los principales FT comercializados en México, los cuales se identificaron como. Inmunoactive®, Terrat®, Transferon® solución oral, Extracto dializado de leucocitos®, Celestine®, G- nomic®; y se asignaron de forma aleatoria con los literales A, B, C, D, E y F.
Cuantificación de proteínas
La cuantificación de proteínas totales en los productos se realizó mediante una técnica colorimétrica utilizando el reactivo de Bradford23 (Sigma-Aldrich™, US) conforme a las instrucciones del fabricante. Para la obtención de las concentraciones de las muestras se realizó un curva-patrón a una concentración máxima de 1 mg/mL, con una solución de albúmina de concentración conocida (Pierce BCA, Protein Assay Kit™, Thermo Fisher Scientific, US). Las absorciones de cada estándar y de las muestras se obtuvieron en un espectrofotómetro Scinco™ S-3100 (Seúl, Corea) a 595 nm. Todas las muestras fueron analizadas por duplicado.
Cromatografía líquida de alto desempeño (HPLC)
El perfil cromatográfico de cada muestra se obtuvo en un HPLC Infinity LC 1220™ (Agilent Technologies, US), con una columna de fase reversa 300-SB-C18 (Zorbax™, Agilent technologies, US), partícula de 5 µm, con dimensiones de 2.1 x 50 mm.
Los cromatogramas fueron generados a 280 nm en un detector ultravioleta (Agilent Technologies, US) a un flujo de 0.8 mL/min-1 de una solución de ácido trifluroacético (TFA), a 0.12% en agua ultrapurificada (Milli Q™, Millipore Corporation, US) y la elución se realizó con un gradiente lineal de una solución de acetonitrilo + TFA a 0.1%. Todas las muestras fueron previamente filtradas y se analizaron por duplicado.
Perfil electroforético en geles de SDS-PAGE
El perfil electroforético de las proteínas en los FT probados se obtuvo según el procedimiento descrito por Laemmli,24 en condiciones desnaturalizantes en un gel de poliacrilamida a 16% de concentración. En cada carril se aplicaron aproximadamente 20 μg de proteínas totales. Los geles fueron teñidos con azul de Coomassie coloidal G-250 con la técnica silver blue.
Las concentraciones proteicas de las diferentes muestras analizadas se observan en la Figura 1. Se muestra el promedio de dos determinaciones independientes.

Figura 1. Análisis del contenido proteico de los FT estudiados, cuantificado por el método de Bradford. Los valores se obtuvieron a partir de una curva de referencia de un estándar de albúmina de concentración conocida.
Las concentraciones de proteínas totales declaradas por los fabricantes de los FT y las obtenidas por cuantificación mediante el método de Bradford se detallan en el Cuadro 1.
| Cuadro 1. Concentraciones de proteínas totales descritas en las etiquetas de los FT analizados y las obtenidas por el método de Bradford | ||
| Factor de transferencia | Concentración declarada por el fabricante | Concentración por cuantificación de proteínas* |
| A | 2.6 μg/mL | 0.098 μg/mL |
| B | NE | 0.094 μg/mL |
| C | 0.4 μg/mL | 0.062 μg/mL |
| D | NE | 0.069 μg/mL |
| E | 92 μg/mL | 0.094 μg/mL |
| F | N/E | 0.118 μg/mL |
| NE, no especificada en el producto; * Método Bradford | ||
Perfil cromatográfico de los FT analizados
Los perfiles cromatográficos representativos para cada uno de los FT analizados se muestran en la Figura 2.
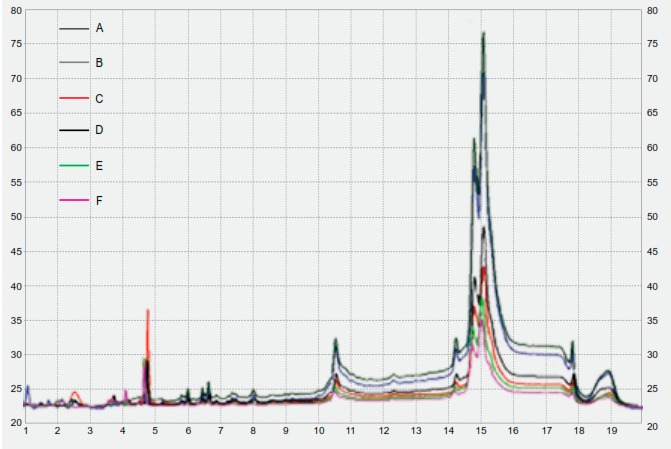
Figura 2. Perfil cromatográfico de los FT analizados, a una absorbancia de 280 nm y a un tiempo de retención de 20 minutos. Los colores en los literales A a F representa cada uno de los FT.
No fue posible obtener los perfiles electroforéticos de los FT analizados, ya que en las condiciones en que se realizó el experimento no se identificaron proteínas en los geles.
En esta investigación analizamos los perfiles proteicos y cromatográficos de seis productos comerciales que contienen factor de transferencia proveniente de leucocitos humanos. Las concentraciones de proteínas totales de las muestras analizadas, determinadas mediante la técnica de Bradford varían en rangos de entre 62 a 118 μg/mL-1, que representan variaciones importantes entre los productos. De cada muestra solo se analizó un lote, por lo que no fue posible determinar la variación de proteínas que pudiera presentarse entre lotes.
Destacó que solamente la mitad de los productos indicaba en su etiquetado o información de insertos la cantidad de proteína contenida en el envase. A partir de esta información se identificó que las concentraciones declaradas con las obtenidas experimentalmente difirieron en magnitud; el producto que presentó mayor diferencia en el FT fue el identificado como E, casi mil veces respecto a la concentración señalada. El producto A presentó una diferencia de 26 veces y el C, de 6 veces. Estas variaciones en la concentración de proteínas entre los diferentes productos analizados podrían tener un impacto terapéutico significativo.
Perfiles cromatográficos
El análisis cromatográfico de las muestras analizadas mostró similitud entre ellas en los tiempos de retención de las fracciones más importantes, con variaciones en la magnitud de los mismos, seguramente como consecuencia de la diferencia en las concentraciones proteicas de las muestras.
Es importante destacar que los componentes principales de los FT se conservaron en la mayoría de los productos, sin embargo, existieron diferencias significativas en varias fracciones menores, principalmente en los tiempos de retención de 1 a 3 minutos. El producto F presentó las mayores variaciones en sus componentes, incluso un ligero desplazamiento en la fracción con tiempo de retención de 4.8 minutos, lo que podría indicar un componente diferente o alguna modificación que pudieran sufrir las proteínas de esa fracción. El producto E mostró también un tiempo de retención distinto en esta fracción, en comparación con lo observado para los otros FT analizados.
Adicionalmente, los productos E y F presentaron variaciones importantes en las fracciones con tiempo de retención de 6 a 8.5 minutos, con ausencia de algunas de ellas o presencia de otras. Si bien esto puede explicarse en parte por las diferencias en las concentraciones de los productos, varias fracciones que no se encontraron en los FT más concentrados fueron claramente componentes diferentes, producto de las variaciones en los procesos de producción o en las fuentes de obtención de los productos. Debido a que se desconoció qué productos fueron los que tuvieron mayor impacto terapéutico, no fue posible establecer la importancia que podrían representar estas diferencias en la seguridad y eficiencia terapéutica.
En cuanto al perfil electroforético, en ninguno de los FT se pudo detectar bandas de proteínas en los geles, probablemente por la técnica empleada para la obtención del perfil y para la tinción del mismo. Sería conveniente emplear para este análisis gel para electroforesis de péptidos y una tinción con plata.
Por último, la revisión de la etiqueta de los productos mostró que ninguno contaba con la información requerida para un producto hemoderivado, como se especifica en la normatividad nacional vigente. La información mínima solicitada en la etiqueta de productos hemoderivados por la Farmacopea de los Estados Unidos Mexicanos25 y su cumplimiento por los fabricantes de FT analizados se describe en el Cuadro 2.
| Cuadro 2. Información escrita proporcionada por los diferentes fabricantes de FT | |||||
| Factor de transferencia | Fuentes de obtención | Concentración de proteínas totales | Lote y caducidad | Registro sanitario | Responsable y lugar de fabricación |
| A | Leucocitaria sin especificación de origen | • | • | • | • |
| B | • | • | Información errónea | • | • |
| C (sublingual) | Leucocitaria sin especificación de origen | • | • | • | • |
| D | • | • | • | • | • |
| E | • | • | • | • | • |
| F | Leucocitaria sin especificación de origen | • | • | • | • |
| • información no descrita en caja o en frasco; • información proporcionada en el empaque o frasco | |||||
Los insumos farmacológicos, biológicos y biotecnológicos para el uso en humanos están regidos por la Farmacopea de los Estados Unidos Mexicanos y las normas oficiales mexicanas NOM-253-SSA1-201226 y NOM-072-SSA1-2012,27 en las cuales se indican los requisitos sobre identidad, pureza, control de calidad de la sangre y sus hemoderivados y su etiquetado; los procesos para su elaboración se encuentran regidos en la NOM-059-SSA1-2015.28
Por tratarse de un producto biológico hemoderivado, el FT debería cumplir con dicha regulación, sin embargo, en ninguno de los empaques o frascos de los 6 productos se indicaba el registro de elaboración y prescripción como medicamento; se declaraban como suplementos alimenticios, aun cuando se empleaban con fines terapéuticos (productos A, B, D, E y F), por lo que tendrían que apegarse a las NOM-SSA1-251-200929 y NOM-051-SCFI/SSA1-2010.30
La normativa vigente también señala que en los hemoderivados se debe describir el contenido de elementos como adyuvantes y contenido de sodio, entre otros. En el análisis efectuado encontramos que únicamente los productos B y E cumplían al menos la descripción de la composición de adyuvantes; el producto E indicaba el contenido de sodio en su etiquetado. Adicionalmente, la NOM-253-SSA1-2012 señala que todos los productos hemoderivados deberán contener en su etiqueta la leyenda ¨la transmisión de agentes infecciosos no es totalmente descartado cuando son administrados productos preparados a partir de la sangre o plasma humano¨, algo que no presenta ninguno de los productos analizados.
Aceptado: 2016-09-21
Correspondencia: Guillermo Guidos-Fogelbach. guillermoguidos@yahoo.com
 Todo el contenido de esta revista, excepto dónde está identificado, está bajo una Licencia Creative Commons
Todo el contenido de esta revista, excepto dónde está identificado, está bajo una Licencia Creative Commons