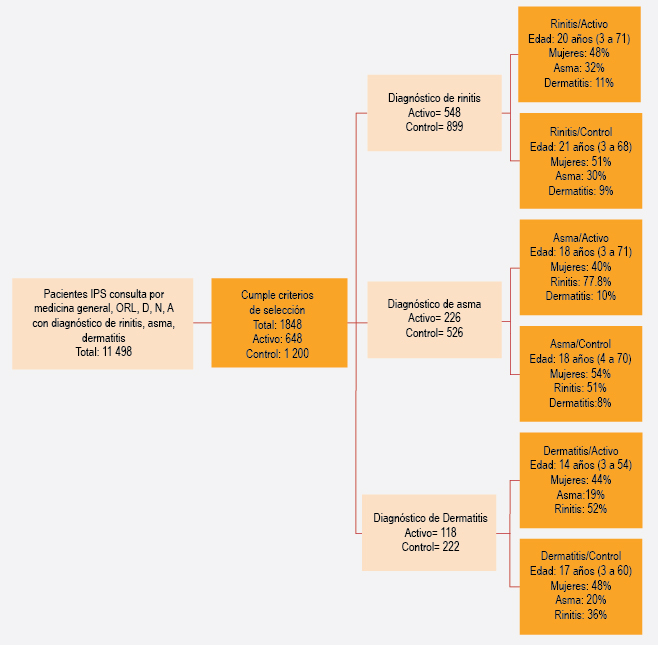
Figura 1. Selección de los pacientes y grupos de acuerdo con la enfermedad. IPS, Instituto Prestador de Salud; ORL, otorrinolaringología; D, dermatología; N, neumología; A, alergología. Se presenta edad media y rango.
ARTÍCULO ORIGINAL
Jorge Sánchez,1-3 Andrés Sánchez,1-4 Ricardo Cardona1
1Universidad de Antioquia, Grupo de Alergología Clínica y Experimental, IPS Universitaria. Medellín, Colombia.
2Fundación para el Desarrollo de las Ciencias Médicas y Biológicas. Cartagena, Colombia.
3Universidad de Cartagena, Instituto de investigaciones Inmunológicas, Grupo de Alergología Experimental e Inmunogenética. Cartagena, Colombia.
4Corporación Universitaria Rafael Núñez. Cartagena, Colombia.
Este artículo debe citarse como: Sánchez J, Sánchez A, Cardona R. Consecuencias económicas en la vida real de la inmunoterapia con alérgenos en asma, rinitis y dermatitis. Rev Alerg Mex. 2016;63(4):323-333.
Antecedentes: La inmunoterapia con alérgenos ha demostrado ser efectiva en el tratamiento de diversas alergias, pero poco se ha evaluado si los beneficios clínicos compensan los costos económicos.
Objetivo: Explorar las consecuencias económicas de la inmunoterapia en asma, rinitis y dermatitis.
Métodos: Estudio retrospectivo analítico. Se seleccionaron pacientes con seguimiento por al menos 18 meses, cuya historia clínica permitiera evaluar los medicamentos recibidos, forma de uso, citas de control, cambios en el tratamiento, motivos de estos, etcétera. Los pacientes fueron clasificados de acuerdo a si recibieron tratamiento farmacológico + inmunoterapia (grupo activo) o solo tratamiento farmacológico (grupo control).
Resultados: 1848 pacientes fueron incluidos: 648 en el grupo activo y 1200 en el control. La inmunoterapia aumentó el costo del tratamiento durante los primeros meses, pero después de 9 a 12 meses disminuyó significativamente el tratamiento farmacológico en comparación con el grupo control. En los pacientes con asma o varias enfermedades, la inmunoterapia redujo los costos del tratamiento (p < 0.05). En el grupo activo se observó menos recaídas a los 18 meses (p < 0.05).
Conclusión: La inmunoterapia con alérgenos permite la reducción sostenida del tratamiento farmacológico, con ahorro económico a mediano plazo para el paciente y el sistema de salud.
Palabras clave: Asma; Análisis costo-beneficio; Dermatitis; Farmacoterapia; Inmunoterapia; Rinitis
How to cite this article: Sánchez J, Sánchez A, Cardona R. [Economic consequences in real life of allergen immunotherapy in asthma, rhinitis and dermatitis]. Rev Alerg Mex. 2016;63 Oct-Dec(4):323-333.
Background: Allergen immunotherapy has proved effective in the treatment of various allergies, but whether the clinical benefits outweigh the economic costs has been little evaluated.
Objective: To explore the economic consequences of immunotherapy in asthma, rhinitis and dermatitis.
Methods: Descriptive study. Patients with at least 18 months’ follow-up were selected, whose medical history allowed evaluation of drugs received, manner of use, check-ups, treatment changes, reasons for these, and so on. Patients were classified according to whether they received drug treatment + immunotherapy (active group) or drug therapy alone (control group).
Results: 1848 patients were included: 648 in the active group and 1200 in the control. Immunotherapy increased the cost of treatment during the first few months, but after 9 to 12 months drug treatment decreased significantly compared to the control group. In patients with asthma or various diseases, immunotherapy reduced costs of treatment (p < 0.05). The active group saw fewer relapses at 18 months (p < 0.05).
Conclusion: Allergen immunotherapy allows the sustained reduction in drug treatment, with medium-term financial savings for the patient and the health system.
Keywords: Asthma; Cost-benefit analysis; Dermatitis; Immunotherapy; Pharmacotherapy; Rhinitis
Abreviaturas y siglas
GHIPS, Gestión Hospitalaria IPS
IgE, inmunoglobulina E
IPS, Instituto Prestador de Salud
Las alergias comprenden un conjunto de enfermedades altamente prevalentes como el asma, la rinitis y la dermatitis, las cuales frecuentemente se presentan de forma simultánea. Cuando los procesos alérgicos no son controlados, pueden dejar secuelas limitantes o poner en peligro la vida de los pacientes. Además del alto costo psicosomático y social, las alergias tienen un alto costo económico que es asumido por el paciente, su familia y el sistema de salud.1
Por lo general, el manejo de las alergias incluye tres modalidades:
De las tres, solo la última tiene un efecto benéfico que perdura años después de terminar el tratamiento,2,3 y permite una reducción significativa (en ocasiones total) del tratamiento antiinflamatorio.4 Por estos y otros efectos, la Organización Mundial de la Salud la considera la piedra angular del tratamiento de las enfermedades alérgicas y la denomina “vacuna para las alergias”, por sus efectos positivos y preventivos, ya que el control inmunomodulador en la rinitis ha demostrado evitar el desarrollo del asma y el agravamiento de los síntomas respiratorios.5,6
Actualmente, en buena parte de los países latinoamericanos se dispone de estudios epidemiológicos que han identificado las principales fuentes de alérgenos asociados con síntomas alérgicos,7-9 por lo que la inmunoterapia es una opción terapéutica viable en la región, si bien es necesario considerar las preferencias del paciente10 y los costos adicionales que genera. De ahí que surja la interrogante de si los beneficios obtenidos de la inmunoterapia justifican el esfuerzo económico adicional para el paciente y el sistema de salud.
En el presente artículo presentamos el análisis de los efectos de la inmunoterapia en cuanto a los costos directos en el tratamiento farmacológico y la atención médica en pacientes con asma, rinitis o dermatitis.
Estudio analítico retrospectivo, realizado en un centro de salud en Medellín, Colombia, en el que se incluyeron pacientes que asistieron a consulta entre 2006 y 2013 y que tuvieron seguimiento hasta enero de 2015.
Fueron seleccionados pacientes con diagnóstico de asma, rinitis o dermatitis, con seguimiento de al menos 18 meses en el centro de salud por un médico especialista en alergología, dermatología, otorrinolaringología o neumología. Fueron excluidos los pacientes con información insuficiente respecto al tratamiento de las enfermedades estudiadas o con comorbilidades crónicas que pudieran influir. Se organizaron en dos grupos: activo y control, de acuerdo a si recibieron o no inmunoterapia. Loso criterios de exclusión fueron no contar con información adecuada respecto a dosificación, motivo del cambio de medicación (en caso de ocurrir), forma de uso (adherencia), frecuencia y regularidad.
Aunque diversos especialistas médicos pueden sugerir la inmunoterapia, en este estudio los pacientes la recibieron por indicación final del alergólogo tratante, dado que en Colombia es aplicada por los alergólogos.
Base de datos
Los datos fueron obtenidos de un centro de referencia (IPS Universitaria, Universidad de Antioquia), el cual tiene, además del Servicio de Alergología, centros de salud que ofrecen atención en neumología, dermatología y otorrinolaringología. En el sistema electrónico de los expedientes clínicos de la institución (Sistema de Gestión Hospitalaria IPS, GHIPS) quedan guardados los datos de cada usuario, los códigos de los diagnósticos y medicamentos prescritos en la consulta, así como otros datos referentes al manejo del paciente. Por ello, la fuente de información para el presente estudio fue el GHIPS.
Se incluyeron pacientes mayores de 3 años que hubieran asistido a la IPS y a quienes se les hubiera diagnosticado asma, rinitis o dermatitis, con al menos seguimiento médico en la IPS durante 18 meses y tres citas de seguimiento:
La historia clínica electrónica debía contar con suficiente información para evaluar los medicamentos recibidos y los cambios en el tiempo, adherencia, dosis, suspensión, esquema de uso y motivos de los cambios. Los pacientes podían tener una o más de las enfermedades estudiadas, en ese caso ingresaron en el análisis de cada una de las enfermedades que tuvieran.
Definición de los grupos
Fueron seleccionados los registros de los pacientes diagnosticados en el centro entre 2006 y 2013. Los pacientes que además del tratamiento farmacológico recibieron inmunoterapia fueron integrados al grupo activo y quienes no recibieron inmunoterapia formaron el grupo control, que solo recibió farmacoterapia.
Para la selección del grupo control se seleccionó a todos los pacientes no expuestos a la inmunoterapia que cumplieron los criterios de selección durante el periodo de estudio, pero se tuvo en cuenta que al menos un paciente del grupo control por cada paciente del grupo activo tuviera una concordancia en las siguientes variables: datos demográficos (edad y sexo), momento diagnóstico de asma, rinitis y dermatitis con diferencia menor a ± 6 meses, periodo de seguimiento y comorbilidades alérgicas.
Para algunas variables demográficas se empleó mediana y rango intercuartílico como medida de dispersión. Se utilizó el Índice de Comorbilidad de Charlson11 (originalmente diseñado para predecir el riesgo de mortalidad en pacientes hospitalizados) para excluir a los pacientes con comorbilidades no alérgicas graves que podían aumentar los costos por causas diferentes a las enfermedades estudiadas, así como la respuesta clínica al tratamiento.
Para cada enfermedad se formaron subgrupos dependiendo de la modalidad terapéutica.
Medición de los costos
Para la evaluación de los costos y la eficacia se consideró el tratamiento recibido al momento del diagnóstico y durante el seguimiento, al igual que el número de citas médicas relacionadas con las enfermedades alérgicas. Se cuantificó la dosis, la frecuencia de uso y las concentraciones de los fármacos. De las variables de costos se obtuvo la mediana y el rango como medida de dispersión. Idealmente a cada paciente se le debía asignar el valor exacto del costo de su tratamiento, sin embargo, por no disponer de la información individual, para cada molécula utilizada en la farmacoterapia se obtuvo el promedio del costo de las diferentes marcas disponibles y se consideraron las fluctuaciones en el precio al público en el año evaluado.
Para determinar el valor ponderativo de cada molécula se tomaron en cuenta las marcas más frecuentemente suministradas por el sistema de salud del país. De igual forma se incluyó el valor por periodo de las citas médicas de control.
Debido a que los pacientes pueden tener múltiples enfermedades (asma, rinitis o dermatitis), se evaluó el costo del tratamiento promedio en la primera y última cita del seguimiento, entre los grupos activo y control. El resultado de estas variables se presentó como el promedio en dólares de acuerdo con la tasa de cambio ponderativo durante el periodo de uso ($1 dólar estadounidense = $2.077 pesos colombianos).
Consideraciones éticas
La información obtenida se ajustó estrictamente a las directrices internacionales de la Declaración de Helsinki, cuidando la privacidad de los pacientes. Se obtuvo autorización del comité de ética de la IPS Universitaria.
Análisis estadístico
En el estudio se evalúo la eficiencia de la inmunoterapia en el tratamiento del asma, la rinitis y la dermatitis. Las variables estudiadas como desenlace primario fueron la reducción en costos de cada enfermedad por separado y el costo por paciente, independientemente del número de enfermedades que tuviera. También se evaluó la suspensión o reducción en el tratamiento recibido entre los grupos activo y control. Los análisis se efectuaron con el programa SPSS versión 21. Las características generales de los pacientes y los resultados se expresaron en porcentajes de frecuencia o en números absolutos. Los costos evaluados estuvieron en relación con el tratamiento utilizado en cada enfermedad, por lo que se compararon los grupos activo y control y de igual forma se integraron subgrupos de acuerdo con los costos de cada enfermedad.
Con las pruebas de Shapiro-Wilk y Kolmogorov-Smirnov se evaluó la distribución y el supuesto de normalidad de las variables de costo y ahorro relacionado (dosis, concentraciones, número de asistencia a centros de salud). Los datos recolectados para las variables de costos y ahorro relacionado no tuvieron distribución normal y se desviaron a la derecha debido a que algunos pacientes sobreutilizaron los servicios de salud y, en consecuencia, los costos se alejaron de la media.
Para corregir los sesgos secundarios a la distribución se utilizó un modelo de regresión lineal generalizada para comparar los costos de atención de los pacientes en cada periodo evaluado con diagnóstico de asma, rinitis o dermatitis que posteriormente recibieron inmunoterapia y fueron emparejados con los de pacientes control que no lo hicieron. Con este modelo también se compararon los ahorros de costos relacionados con la inmunoterapia durante los 18 meses de seguimiento y se analizaron los subgrupos conforme a las enfermedades incluidas.
De acuerdo con la variable evaluada se empleó chi cuadrada para las variables dicotómicas (sí o no en la reducción de la concentración de la medicación y en el costo del tratamiento), regresión logística (variables categóricas reducción de costo, reducción de medicación), grupo (activo versus control) y correlación (costo neto versus concentración de medicación). Algunas variables fueron tratadas de forma continua o categórica de acuerdo con el análisis realizado (ejemplo, análisis de chi cuadrada para sí o no en la reducción del costo y análisis de correlación para valor neto de la reducción). Cuando fue pertinente se hizo análisis de regresión logística multivariada, con ajuste por edad y sexo. Se consideró significativo un valor de p < 0.05.
Características de la población
Se revisaron 11 498 ingresos, de los cuales 1848 pacientes cumplieron con los criterios de selección (Figura 1). Entre las comorbilidades que motivaron la exclusión de 400 pacientes estuvieron las enfermedades coronarias no controladas (35%), cerebrovasculares (30 %) y otras (25%). El rango de edad fue de 3 a 69 años (promedio 21 años); 52% era del sexo femenino, 37% tenía dos o más de las enfermedades estudiadas, tanto en el grupo control (n = 447) como en el activo (n = 244), que fue incluido en cada uno los grupos correspondientes cuando el análisis se hizo por enfermedades. En la Figura 1 se presentan los grupos de acuerdo con la enfermedad tomando en cuenta la media y los rangos de edad. Al evaluar los grupos de acuerdo con la mediana y los percentiles 25-75 encontramos los siguientes valores: rinitis en el grupo activo 19 (6-63) y en el control 20 (6-62); asma en el grupo activo 18 (6-62); dermatitis en el grupo activo 15 (5-50) y en el control 17 (5-54).

Figura 1. Selección de los pacientes y grupos de acuerdo con la enfermedad. IPS, Instituto Prestador de Salud; ORL, otorrinolaringología; D, dermatología; N, neumología; A, alergología. Se presenta edad media y rango.
Costo del tratamiento por enfermedad
En la cita 1, el grupo activo tuvo un gasto mayor en el tratamiento que el grupo control para las tres enfermedades (Cuadro 1). Este costo adicional estuvo directamente ligado a la inmunoterapia, que representó 17% del costo del tratamiento en el grupo activo con asma, 35% con rinitis y 18% con dermatitis.
| Cuadro 1. Gasto promedio por paciente en el periodo de tiempo de acuerdo con cada enfermedad | ||||
| Enfermedad | Cita 1 (Inicial) | Cita 2 (3-6 meses) | Cita 3 (7-12 meses) | Cita 4 (13-18 meses) |
| Asma/Activo | 339 (90-3.092) | 253 (81-2.942) | 210 (585-2.613) | 174* (71-2.512) |
| Asma/Control | 287** (32-3.009) | 215* (248-2.897) | 238 (37-2.845) | 221 (59-2.892) |
| Rinitis/Activo | 162 (93-297) | 133 (84-257) | 114 (74-127) | 94 (70-102) |
| Rinitis/Control | 109** (40-232) | 79** (43-230) | 79* (74-225) | 74 (33-243) |
| Dermatitis/Activo | 320 (100-4.964) | 293 (95-454) | 249 (86-371) | 233 (75-396) |
| Dermatitis/Control | 243** (40-613) | 212** (45 -606) | 229* (40-486) | 219 (35-446) |
| Varios pacientes tenían al mismo tiempo asma, rinitis o dermatitis. Para cada enfermedad, el costo fue evaluado por separado y presentado en pesos. El valor en el grupo activo incluye la inmunoterapia. Grupo control activo por enfermedad: **< 0.01, *<0.05. Se señala significación (*) en grupo con menor costo. | ||||
Durante el seguimiento, todos los grupos tuvieron una reducción en los costos del tratamiento debido a la reducción de las dosis o la suspensión de medicamentos, la cual fue mayor en las citas 3 y 4 en el grupo activo para cada enfermedad. Para la rinitis y la dermatitis, el gasto neto por periodo fue mayor que en los grupos control de cada enfermedad hasta la cita 3; posteriormente, la diferencia no fue estadísticamente significativa. Para el grupo con asma, la reducción en los costos luego de 12 meses del tratamiento fue significativamente mayor en el grupo activo (p < 0.05).
Reducción de la medicación durante el seguimiento
De acuerdo con la respuesta clínica de cada paciente al tratamiento instaurado en la cita previa, el médico tratante ajustaba el tratamiento en la cita siguiente (aumentando la medicación, dejándola igual o reduciéndola). Todos los grupos presentaron reducción en el tratamiento farmacológico en la cita 2 (Figura 2). En los grupos con inmunoterapia, la reducción de los medicamentos fue sostenida en las tres citas de seguimiento, mientras que en los grupos control, la reducción fue menor y en la cita 3 fue necesario aumentar el tratamiento farmacológico en un grupo. Esta diferencia entre los grupos control y activo fue más evidente en la cita 4.
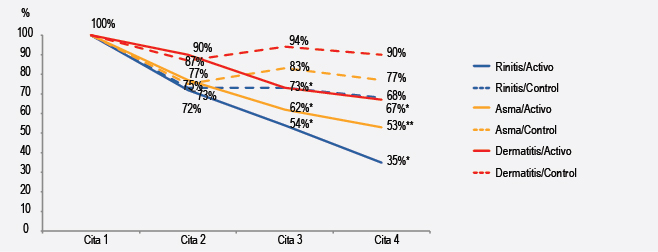
Figura 2. Reducción del tratamiento farmacológico. Cita 1, primera cita; cita 2, 3 a 6 meses; cita 3, 7 a 12 meses; cita 4, 13 a 18 meses. *< 0.05, **< 0.01.
Al evaluar mediante regresión logística multivariable si la edad (≤ 14 años o > 14 años) influía en los resultados, se observó que los pacientes ≤ 14 años con enfermedades respiratorias tenían una reducción sostenida mayor del tratamiento (p = 0.04) independientemente del sexo.
Gasto global por paciente
Un 37% de los pacientes presentó múltiples enfermedades (asma, rinitis o dermatitis). Al inicio del estudio, el grupo activo tenía un sobrecosto frente al grupo control de 33 a 23% debido a la inmunoterapia. Al final de la evaluación, la reducción de los medicamentos y del número de citas fue significativa en el grupo activo comparado con el grupo control (Figura 3). Al comparar la suspensión de medicamentos (Figura 4) en el último periodo por más de 3 meses debido a un buen control y sin recaídas, la reducción fue mayor en el grupo activo en comparación con el control para rinitis (9% versus 5%), asma (8% versus 4%) y dermatitis (2 versus 1%), siendo estadísticamente significativa para las enfermedades respiratorias. Dado que numerosos pacientes padecían múltiples enfermedades, se compararon los grupos activo y control independientemente de las enfermedades base; se observó una suspensión mayor del tratamiento farmacológico en el grupo activo (12% versus 6%).
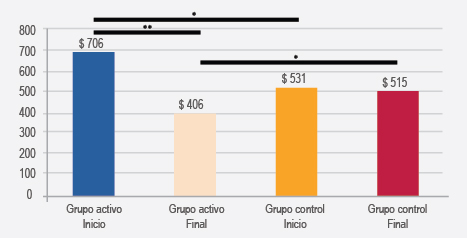
Figura 3. Costo global del tratamiento. *< 0.05, **< 0.01.
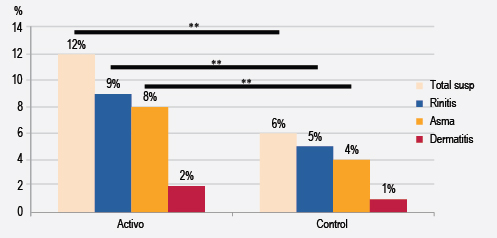
Figura 4. Pacientes con suspensión de medicamentos al final del estudio. Total susp, pacientes con suspensión total de la farmacoterapia; %, pacientes independientemente de la enfermedad de base. **< 0.01, *< 0.05.
La farmacoterapia es ampliamente usada en asma, rinitis y dermatitis. En la mayoría de las ocasiones suele ser efectiva para controlar los síntomas, sin embargo, no cambia el curso de las alergias y no previene el aumento en su prevalencia. La identificación de las fuentes causantes de los síntomas permite implementar medidas encaminadas a reducir la exposición a los alérgenos, sin embargo, en algunas sustancias suelen ser insuficientes para controlar completamente los síntomas.12,13 Cuando los mecanismos causantes de los síntomas tienen una mediación IgE, la inmunoterapia con alérgenos consigue mejorar el control de los síntomas de los pacientes atópicos y genera tolerancia inmunológica con efecto a largo plazo,14-17 previniendo el progreso en la gravedad de los síntomas y el desarrollo de nuevas alergias.
Una dificultad para determinar el éxito de la inmunoterapia es el consecuente costo adicional, sin embargo, los resultados de este estudio muestran que el costo extra inicial suele ser compensado luego de 9 a 12 meses por el mejor control del asma, la rinitis y la dermatitis, que permite una reducción sostenida de los medicamentos.
Aunque el estudio de costos de un tratamiento para una enfermedad determinada debería hacerse en pacientes con solo una enfermedad, la presencia de varias enfermedades tipo IgE mediadas es muy común en los pacientes alérgicos y es infrecuente encontrar pacientes con solo dermatitis, rinitis o asma. Por eso, los análisis realizados en este estudio incluyen la evaluación de costos del tratamiento tanto por cada enfermedad como por paciente, ya que cada uno puede tener diferentes combinaciones de estas enfermedades y, por tanto, diferentes tipos y costos de tratamiento.
Teniendo en cuenta que estas enfermedades suelen ser crónicas, la reducción de la farmacoterapia secundaria a un buen control sintomático puede generar importantes ahorros para el sistema de salud y el paciente. En el asma, su alta prevalencia18 la hace una enfermedad de alto costo tanto por los medicamentos de control como por las visitas a urgencias. Debido a que 60 a 80% de los pacientes con asma padece rinitis, los costos del tratamiento se incrementan y se dificulta el control de los síntomas.19 Las alergias respiratorias están asociadas con ausentismo laboral o escolar, déficit de atención y, en el caso del asma, muerte por exacerbaciones no controladas.20,21 Junto al impacto psicosocial, el ausentismo, las hospitalizaciones, la asistencia a urgencias y otros procesos secundarios generan una importante carga económica para el paciente y el sistema de salud.22
En otras investigaciones se ha observado que después de un año de tratamiento, los pacientes presentan un mejor control de los síntomas, lo que permite reducir con pocas recaídas la farmacoterapia hasta en 30 a 45%.23-26 En forma similar a nuestra investigación, esos estudios indican que aun cuando en los primeros meses el costo del tratamiento para asma o rinitis aumenta por la inmunoterapia, a mediano plazo este costo se reduce significativamente, incluso, el costo llega a ser menor que en los pacientes que solo reciben el tratamiento farmacológico. Es importante anotar que esta reducción es secundaria al mejor control de los síntomas, lo que potencialmente implica menor número de asistencias a urgencias y hospitalizaciones, mejoría en la calidad de vida de los pacientes y menor riesgo de efectos adversos por la farmacoterapia.
Algunos estudios han demostrado que la aplicación de la inmunoterapia en los niños con rinitis alérgica reduce significativamente el riesgo de desarrollar posteriormente asma o conjuntivitis, por lo que en ellos la inmunoterapia es activa y preventiva, reduciendo los costos socioeconómicos secundarios.3 Igualmente, para conseguir el mejor éxito es necesario seleccionar adecuadamente a los pacientes y que el tratamiento sea aplicado por personal experto.
La dermatitis atópica afecta a 5% de la población infantil y a 1 de cada 100 adultos. Puede afectar severamente y en ocasiones de manera irreversible la piel, por lo que entre las enfermedades alérgicas es la que más se relaciona con trastornos psicológicos, baja autoestima, depresión e ideación suicida.27 Además, se ha observado que los niños menores de 2 años de edad con dermatitis atópica tienen un riesgo 6 a 8 veces mayor de desarrollar asma y otras alergias. Actualmente, varias guías sobre dermatitis han incluido la inmunoterapia como una herramienta en el manejo de esta enfermedad con base en estudios controlados que señalan que su uso en los pacientes con dermatitis moderada o severa disminuye el requerimiento de medicamentos tópicos y sistémicos, cuyo empleo crónico frecuentemente ocasiona efectos adversos.14,28,29
Los resultados de esta investigación muestran que la inmunoterapia genera un costo adicional importante en el tratamiento de la dermatitis, sin embargo, al igual que en el asma y la rinitis, el costo se reduce significativamente entre los 9 y 12 meses y el gasto total es similar al del grupo control.
Aunque al evaluar por separado el gasto para la rinitis y la dermatitis, los grupos control tuvieron un gasto levemente inferior que los grupos activos en la última cita, la mayoría de los pacientes con dermatitis, al igual que buena parte de aquellos con rinitis, tenía varias enfermedades alérgicas y al evaluar el costo global del tratamiento en el grupo activo hubo mayor ahorro, el cual fue sostenido en el grupo de pacientes con inmunoterapia, ya que una menor cantidad requirió aumento de dosis en comparación con el grupo control y mayor proporción suspendió completamente la farmacoterapia.
Nuestro estudio tiene algunas debilidades propias de los análisis retrospectivos: para evaluar el control clínico hubiera sido adecuado utilizar una escala unificada de control de síntomas para cada enfermedad, sin embargo, el monitoreo de la dosis administrada de farmacoterapia es un parámetro frecuentemente utilizado para evaluar la mejoría clínica.
Otro aspecto fue que al analizar los datos de un solo centro de salud especializado, la mayoría de los pacientes atendidos padecía cuadros severos o de difícil control, lo cual se reflejó en un costo mayor del tratamiento en comparación con los pacientes con síntomas leves atendidos en centros de atención primaria, por lo que los resultados hubieran sido más sólidos si el estudio hubiera sido multicéntrico. No obstante, la población con síntomas más severos presenta una oportunidad: son precisamente los pacientes con cuadros severos los que más se pueden beneficiar de la inmunoterapia y quienes incurren en mayores gastos económicos.
Debido a las limitaciones en la fuente de información, los gastos en citas a urgencias no pudieron ser evaluadas, pero hubo menor reporte de exacerbaciones que requirieron urgencias en las historias clínicas de los pacientes con asma que recibían inmunoterapia (datos no mostrados), lo que hace pensar que además de menor necesidad de tratamiento farmacológico, la inmunoterapia puede tener un impacto importante en reducir las exacerbaciones.
Por al amplio surtido de medicamentos y marcas actualmente disponibles para el manejo de las enfermedades estudiadas, el valor asignado fue obtenido del promedio de los precios para las marcas más usadas de cada molécula. Esta medida limita proporcionar el costo exacto del tratamiento en cada paciente, pero al ser utilizado el mismo parámetro en los grupos control y activo para todos los medicamentos no afectó la evaluación de las diferencias observadas.
En conclusión, estos resultados ―al igual que los obtenidos sobre eficacia en estudios nacionales e internacionales― sustentan a la inmunoterapia como clínicamente efectiva y segura y que luego de un año reduce sustancialmente el costo global del tratamiento de las enfermedades alérgicas severas.
No obstante lo anterior, es necesario realizar estudios preferentemente prospectivos y multicéntricos que incluyan pacientes con síntomas leves para confirmar estos resultados y caracterizar a la población blanco.
El presente artículo fue financiado por los autores.
A la doctora Elizabeth López por su apoyo en la recolección de los datos.
Recibido: 2016-01-17
Aceptado: 2016-03-24
Correspondencia: Jorge Sánchez. jotamsc@yahoo.com
 Todo el contenido de esta revista, excepto dónde está identificado, está bajo una Licencia Creative Commons
Todo el contenido de esta revista, excepto dónde está identificado, está bajo una Licencia Creative Commons